 NUEVOS ALIMENTOS en la UE
NUEVOS ALIMENTOS en la UE
En la UE, los nuevos alimentos (NF) se clasifican, según el Reglamento (UE) 2015/2283, como productos que no han sido ampliamente consumidos en la UE antes de mayo de 1997. Estos alimentos no pueden comercializarse antes de la autorización de la Comisión Europea (CE).
Para comercializar productos de CBD, clasificados como nuevos alimentos en el mercado de la UE, un operador comercial debe presentar una solicitud a la CE para la autorización de este producto en particular. La tramitación de la solicitud es compleja y consta de los siguientes pasos:
- En el paso inicial, la Comisión Europea (CE) y la Autoridad Europea de Seguridad Alimentaria (EFSA) realizan una comprobación de validez de la solicitud de NF presentada. Una vez que el solicitante presenta toda la información requerida, se confirma la validación de la solicitud de NF.
- El siguiente paso es una evaluación del riesgo por parte de la EFSA, que suele ser solicitada por la CE. La EFSA expresa su opinión sobre el nuevo alimento en un plazo de 9 meses si no hay más solicitudes de las autoridades en esta etapa.
- En un plazo de 7 meses a partir del dictamen de la EFSA, la CE presenta un proyecto de acto de ejecución que autoriza la comercialización legal del nuevo alimento.
- Una vez que el acto recibe el voto favorable del Comité Permanente y es adoptado por la CE, la NF puede ser colocada legalmente en el mercado de la UE.

NUEVOS ALIMENTOS en el Reino Unido
El sistema de autorización de las NF es similar en el Reino Unido en lo que respecta a la legislación sobre las NF. Sin embargo, cuando se trata de productos de CBD, la Agencia de Normas Alimentarias (FSA) decidió actuar de forma un poco diferente.
El 13 de febrero de 2020, las autoridades anunciaron que las empresas que venden productos de CBD en el Reino Unido deben presentar y tener una solicitud de NF validada antes del 31 de marzo de 2021. Después de esta fecha, sólo se permitirá que permanezcan en el mercado los productos para los que la FSA haya revisado y asignado la solicitud correspondiente como válida.
Esto ha cambiado en marzo de 2021, cuando la FSA anunció que las empresas sólo tienen que presentar las solicitudes de NF para finales de marzo de 2021.
La FSA también estableció una llamada “lista pública”, que proporciona información pública sobre los solicitantes que tienen sus solicitudes NF válidas. La FSA afirma claramente que el proceso se desarrolla en paralelo al proceso de validación de las solicitudes de NF que se está llevando a cabo en la actualidad y no afecta al resultado del estado de validación.
Por el momento, todas las empresas pueden vender sus productos de CBD en el Reino Unido, siempre que no estén incorrectamente etiquetados, no sean inseguros y estén contemplados en sus correspondientes solicitudes de NF que fueron presentadas antes de marzo de 2021.
PHARMAHEMP – ESTADO DE LAS NUEVAS APLICACIONES ALIMENTARIAS
Estamos en proceso de autorización de dos nuevos ingredientes alimentarios, concretamente el cannabidiol (CBD) y el extracto de Cannabis sativa L. Ambas solicitudes fueron presentadas a la CE en la UE y a la FSA en el Reino Unido en 2020 y 2021.
Estado actual de la CE:
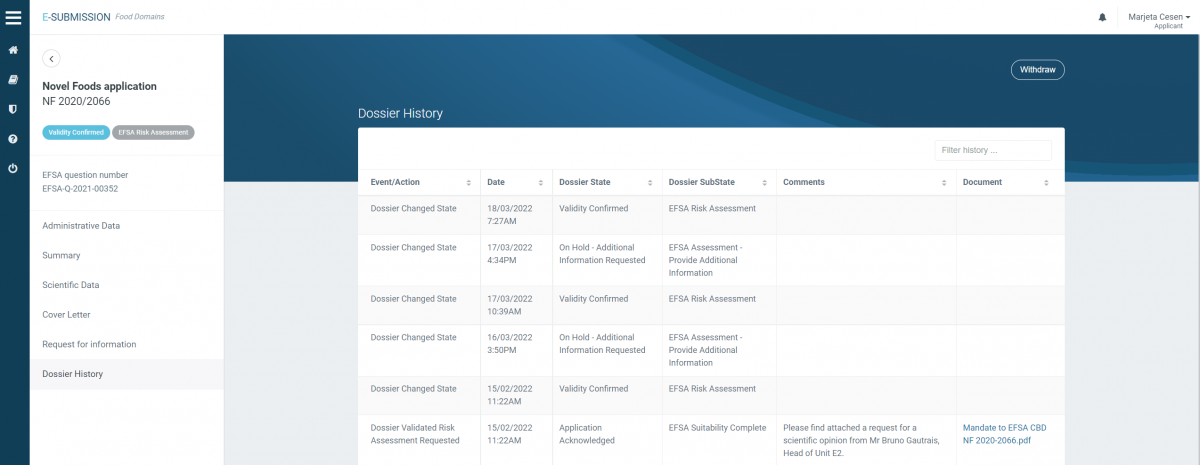
Solicitud de nuevos alimentos para CBD (2020/2066) = Válido desde febrero de 2022
Nueva solicitud de alimentos para el extracto de Cannabis sativa L. NF (2020/2177) = Válido desde febrero de 2022
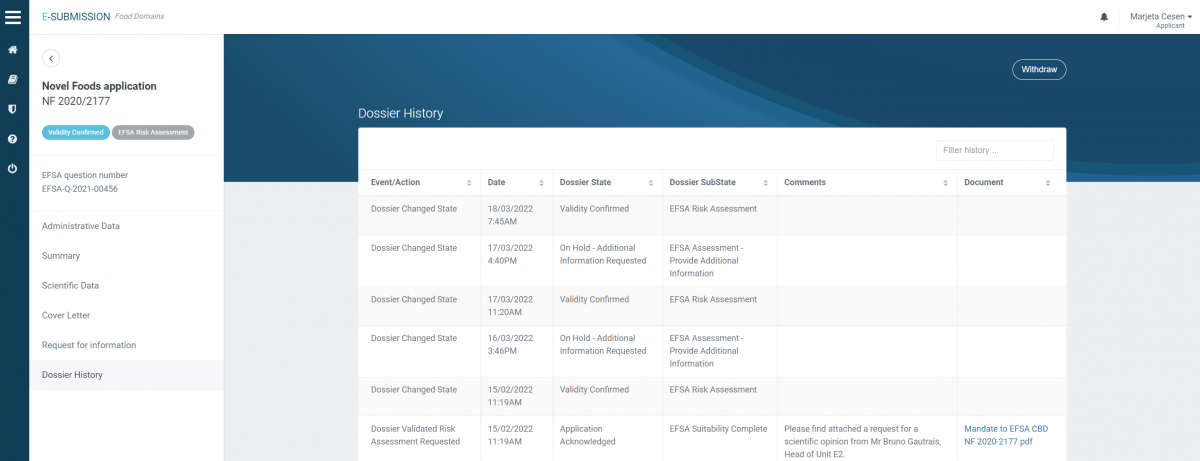
El estado de las nuevas aplicaciones alimentarias también está disponible públicamente en OpenEFSA Portal.
Estado actual del Reino Unido:
Nueva solicitud de alimentos para el extracto de Cannabis sativa L. (RP-821) = validado (en la fase de evaluación de riesgos)
545 productos que están relacionados con la solicitud RP-821 de PharmaHemps de la NF aparecen en la lista pública de CBD creada por la Agencia de Normas Alimentarias.










